Лечение малярии: дозировки, схемы и особенности применения
Профессиональное руководство по лечению малярии. Актуальные схемы терапии, выбор препаратов и дозировки для взрослых, детей и беременных. Ведение тяжелых форм инфекции.
Специальности
АкушерствоАнгиологияАнестезиологияГастроэнтерологияГематологияГепатологияГинекологияГистологияДерматологияИнфекционные болезниКардиологияНеврологияОнкологияОртопедияОториноларингологияОфтальмологияПедиатрияПульмонологияСтоматологияТравматологияУрологияФизиологияЭмбриологияЭндокринологияЭта статья предназначена только для информационных целей
Содержание этого сайта, включая текст, графику и другие материалы, предоставляется исключительно в информационных целях. Оно не является советом или руководством к действию. По поводу вашего конкретного состояния здоровья или лечения, пожалуйста, проконсультируйтесь с вашим лечащим врачом.
Заболевания, вызванные цестодами (цестодозы) — это группа паразитарных заболеваний, вызываемых ленточными червями (цестодами), которые поражают кишечник человека и, в некоторых случаях, внутренние органы и центральную нервную систему. В данной статье рассмотрены наиболее клинически значимые из них: тениоз и цистицеркоз, дифиллоботриоз, а также гименолепидоз и дипилидиоз.
Тениоз — одно из ведущих паразитарных заболеваний, передающихся через пищу. С 2010 г. Всемирная организация здравоохранения (ВОЗ) классифицирует его как забытое тропическое заболевание.
Возбудители — ленточные черви из семейства Taeniidae (подкласс Eucestoda, отряд Cyclophyllidea): Taenia saginata (бычий ленточный червь), Taenia solium (свиной ленточный червь) и Taenia asiatica (азиатский ленточный червь).
Факторы высокого риска инфицирования человека — особенности системы сельскохозяйственного производства, культура питания и обычаи населения, неудовлетворительные санитарные условия и низкий уровень личной гигиены (открытая дефекация, использование для питья воды из небезопасных источников и употребление недостаточно термически обработанной зараженной свинины или говядины и продуктов из них).
![Жизненный цикл Taenia. Источник: CDC (DPDx) [2]](https://storage.googleapis.com/dev_wiki_voka_io_303011/articles/en/infectious-diseases/cestode-borne-diseases/1-taenia-life.webp)
![Жизненный цикл Taenia. Источник: CDC (DPDx) [2]](https://storage.googleapis.com/dev_wiki_voka_io_303011/articles/en/infectious-diseases/cestode-borne-diseases/1-taenia-life.webp)
Человек — единственный окончательный хозяин для трех видов гельминта. Крупный рогатый скот — промежуточный хозяин для T. saginata, свиньи — хозяева личинок T. solium и T. asiatica.
Этапы жизненного цикла:
Взрослые особи T. saginata обычно имеют до 2000, а иногда до 5000 члеников. Из каждого членика может выделяться до 100 000 яиц. T. solium имеет около 1000 члеников, а каждый членик содержит до 50 000 яиц. T. asiatica достигает размеров 4–8 м, один червь состоит в среднем из 700 члеников, а из членика могут выделяться до 80 000 яиц.


По данным ВОЗ, в мире от тениоза страдают более 500 млн человек. Показатель смертности достигает 50 000 случаев в год. Частота заболевания в Европе составляет 0,05–0,27 %, в Африке, Азии и Латинской Америке — до 17,25 %.
T. saginata и T. solium распространены по всему миру, но чаще встречаются в бедных общинах, где люди живут в тесном контакте со свиньями и употребляют в пищу недостаточно прожаренную свинину или говядину. В Восточной Африке распространенность тениоза, вызываемого T. solium, составляет 14–20 % (например, в Танзании средняя серопревалентность — около 17 %, в 2012 г. здесь было зарегистрировано 212 летальных исходов и 17 853 случая нейроцистицеркоза). T. asiatica встречается только в Азии, преимущественно в Корее, Китае, Индонезии, Таиланде и на Тайване.
Из-за больших размеров взрослых червей инфекция, вызванная T. saginata, чаще сопровождается симптомами, чем инфекция, вызванная T. solium или T. asiatica. Тениоз, как правило, протекает бессимптомно или с легкими неспецифическими абдоминальными симптомами, такими как дискомфорт в эпигастральной области, тошнота, метеоризм, диарея или чувство голода. Наиболее характерная особенность — выход члеников: активный (концевые зрелые членики, оторвавшиеся от стробилы, подвижны и могут выползать из кишечника через анальный проход) и пассивный (выделение с каловыми массами во время дефекации). В редких случаях миграция члеников может привести к аппендициту или холангиту.
Особенность тениоза, вызываемого T. solium, — риск развития цистицеркоза (полиорганной глистной инвазии) вследствие проглатывания яиц T. solium. Проглоченные онкосферы созревают, проникают через стенку кишечника, попадают в кровоток и транспортируются в различные органы, включая ЦНС, мышцы, подкожную ткань и глаза. Люди с тениозом могут самоинфицироваться цистицеркозом фекально-оральным путем и представляют эпидопасность для окружающих (у каждого пятого человека с цистицеркозом отмечается сопутствующий тениоз — наличие взрослых червей в кишечнике).
Нейроцистицеркоз (НЦЦ, или цистицеркоз головного мозга) — наиболее распространенная паразитарная инфекция центральной нервной системы. Она характеризуется развитием кист в головном мозге, является причиной 30 % случаев приобретенной эпилепсии в эндемичных районах, что приводит примерно к 61–212 смертельным исходам ежегодно в странах Восточной Африки. В странах Африки к югу от Сахары от симптоматического нейроцистицеркоза страдают около 0,95–3,08 млн человек.
Симптомы заболевания разнообразны и варьируют в зависимости от локализации кисты, стадии ее развития, количества кист и (редко) размера взрослого гельминта. Наиболее распространенные признаки: судороги, гидроцефалия (синдром Брунса — выраженная головная боль, головокружение и рвота при изменении положения головы или тела, чаще при наклоне головы вперед), изменение ментального статуса (прогрессирующая деменция), неврологический дефицит.
Паренхиматозный цистицеркоз (внутрипаренхиматозные кисты) локализуется в перивентрикулярном белом веществе, базальных ганглиях, а также на границе серого и белого вещества. Экстрапаренхиматозный цистицеркоз (рацемозная форма нейроцистицеркоза) представляет собой многокамерные экстрааксиальные кисты, напоминающие «гроздь винограда», и локализуется в субарахноидальных пространствах и желудочках, особенно в четвертом желудочке. Поражение спинного мозга встречается редко и проявляется лептоменингеальной или интрамедуллярной формой, возникающей в результате миграции личинок через субарахноидальное пространство или сосуды соответственно.
Диагностическая ценность микроскопии кала ограничена (чувствительность составляет 38–69 %) из-за нерегулярного выхода члеников и сходства яиц у разных видов Taenia. Метод неприменим в течение первых трех месяцев после инфицирования, то есть до развития взрослых ленточных червей. Для повышения чувствительности рекомендуется исследовать три образца кала, собранных в разные дни. Яйца Taenia spp. также неотличимы от яиц Echinococcus.
Микроскопическая идентификация зрелых члеников позволяет определить вид гельминта. В члениках, расположенных на конце стробилы, атрофируется большая часть половых органов, а матка значительно увеличивается в размерах, накапливая оплодотворенные яйца. Такие членики называют зрелыми. Они имеют прямоугольную форму, длину 16–20 мм и ширину 4–7 мм.
Количество боковых ответвлений с каждой стороны среднего ствола матки в зрелом членике составляет:
Серологические методы особенно актуальны на ранних стадиях заболевания, когда яйца и членики еще не обнаруживаются в кале. Однако их чувствительность низка при единичных поражениях и кальцинированных кистах. При множественных паренхимальных поражениях, а также при субарахноидальном и внутрижелудочковом НЦЦ чувствительность достигает почти 100 %. Титры антител быстро снижаются после терапии.
Эволюционные стадии цистицерка в головном мозге:
Биопсия головного мозга — окончательный способ установить НЦЦ (редко осуществима).


Дифиллоботриоз — паразитарная инфекция, вызываемая широкими или рыбьими ленточными червями.
Возбудителями дифиллоботриоза у человека являются шесть видов ленточных червей, относящихся к трем родам: Dibothriocephalus, Diphyllobothrium и Adenocephalus.
К ним относятся:
Специфичность к определенному хозяину среди имеющих медицинское значение дифиллоботриид низкая. Помимо человека, в качестве окончательных хозяев могут выступать и другие плотоядные, рыбоядные млекопитающие, а также некоторые птицы. Промежуточные и паратенические хозяева для D. latus — разнообразные пресноводные и морские рыбы (чаще окунь, хек и щука), для D. nihonkaiense — лососевые. Окончательные хозяева D. latus, D. nihonkaiense и D. dendriticus — различные плотоядные млекопитающие (псы, кошачьи, медведи и куньи). Ластоногие, собаки и шакалы — окончательные хозяева A. pacificus. D. stemmacephalum встречается в основном у дельфинов и морских свиней, D. balaenopterae — у китов.
Фактор высокого риска инфицирования человека — регулярное употребление или дегустация сырой рыбы в рамках местной кухни (копченой, соленой, севиче, суши и других продуктов).
Точная оценка распространенности затруднена из-за отсутствия обязательной отчетности в большинстве стран. Учитывая преимущественно бессимптомное течение или легкие неспецифические симптомы, недостаточная диагностика дифиллоботриоза весьма вероятна. В 2002 г. мировая распространенность заболевания оценивалась в 20 млн человек.
D. latus имеет относительно широкое географическое распространение, но наиболее часто встречается в приполярных регионах, эндемичен для озер субарктических и умеренных широт Евразийского континента, но очень редко встречается в Южной Америке. D. nihonkaiense — эндемик северной части Тихого океана, случаи заболевания распространены в странах Восточной Азии. D. dendriticus наиболее распространен в Арктике. Подавляющее большинство случаев A. pacificus приходится на тихоокеанское побережье Южной Америки. D. stemmacephalum и D. balaenopterae распространены повсеместно.
Инфекции встречаются преимущественно в странах и регионах, где традиционная кухня предполагает употребление сырой рыбы (копченой, маринованной, в виде суши, севиче и других блюд). Рост миграции населения, путешествий, быстрая транспортировка охлажденной рыбы на большие расстояния из эндемичных стран, популярность блюд из сырой рыбы приводят к регулярным случаям заболевания людей за пределами эндемичных регионов. Неэффективная очистка сточных вод может играть важную роль в поддержании обширных популяций Diphyllobothriidae. Высокий уровень инфицирования усугубляется ограниченным доступом к надлежащим санитарным условиям, улучшение которых способствовало искоренению D. latus (Великобритания, Австрия, Чехия, Бельгия и Нидерланды больше не считаются эндемичными).


Жизненные циклы ленточных червей семейства Diphyllobothriidae сложны, и полный жизненный цикл известен лишь для немногих видов. Все Diphyllobothriidae, вызывающие заболевания у людей, имеют морской или водный жизненный цикл, а передача происходит при употреблении в пищу недостаточно термически обработанной рыбы. Чаще всего личинки проходят через двух промежуточных хозяев, прежде чем ленточный червь созреет в кишечнике окончательного или случайного хозяина. Человек, по-видимому, является основным окончательным хозяином только для D. latus и, возможно, для D. nihonkaiense.
Этапы жизненного цикла:
В большинстве случаев заболевание протекает бессимптомно. Взрослые черви могут обнаруживаться случайно при колоноскопии или при выделении члеников. Примерно у 25 % пациентов могут наблюдаться легкие неспецифические желудочно-кишечные симптомы (диарея, абдоминальная боль или дискомфорт, вздутие, запор) или аллергические реакции. Длительная или тяжелая инвазия часто приводит к развитию дефицита витамина В12 (диагностируется примерно в 40 % случаев), анемия встречается редко (менее 2 % случаев). Иногда при аномальном прикреплении сколекса или высокой паразитарной нагрузке могут развиться кишечная непроходимость, холангит, аппендицит и холецистит.




Микроскопическое определение яиц в кале — золотой стандарт диагностики Diphyllobothriidae на уровне семейства. Отсутствие видоспецифических морфологических признаков и внутривидовая изменчивость характеристик яиц у широкого спектра видов ленточных червей затрудняют идентификацию по яйцам на уровне рода. Для идентификации вида применяется ПЦР-диагностика (в настоящее время, как правило, используется только в исследовательских целях, поскольку схема терапии одинакова для всех видов и точная видовая диагностика клинически не требуется).
Яйца обычно многочисленны: на одного червя в день может приходиться до 1 млн яиц. Они могут быть обнаружены без использования методов обогащения (концентрирования). Идентификация члеников, выделяемых с калом, также имеет диагностическое значение. Если был выделен большой сегмент гельминта, в течение нескольких месяцев яйца в кале могут отсутствовать, поэтому может потребоваться повторное исследование.
Серологическая диагностика Diphyllobothriidae не разработана.
Визуализация предполагает УЗИ кишечника, при котором визуализируется свободно плавающее в просвете лентообразное образование, а также колоноскопию и МРТ органов брюшной полости. Однако эти методы не являются основными в диагностике.
Изолированный дефицит витамина В12 купируется только на фоне противопаразитарной терапии.
Следует избегать употребления рыбы, которая не прошла достаточную термическую обработку или не была правильно заморожена (особенно это касается сырой, маринованной, копченой и сушеной рыбы). Центры по контролю и профилактике заболеваний США (CDC) рекомендуют готовить рыбу до внутренней температуры не менее 63 °C.
Адекватная заморозка и паразитологическое обследование рыбы перед экспортом могут способствовать предотвращению глобального распространения видов Diphyllobothriidae. Рыбу следует замораживать до полного промерзания (простое охлаждение на льду неэффективно) и хранить при очень низкой температуре в течение времени, необходимого для уничтожения плероцеркоидов:
Замачивание в 12 % растворе NaCl также убивает личинки плероцеркоидов.
Гименолепидоз — паразитарное заболевание, вызываемое двумя видами цестод: Hymenolepis nana и Hymenolepis diminuta. H. nana — карликовый ленточный червь длиной 1,5–4 см. Для завершения жизненного цикла ему требуется только один хозяин (но возможен цикл с участием двух хозяев). H. diminuta — крысиный ленточный червь длиной 20–60 см, у людей встречается редко.
H. nana и H. diminuta встречаются во всем мире среди людей (в первую очередь детей), живущих в условиях бедности и плохой гигиены. Точное число случаев заболевания гименолепидозом у человека в мире неизвестно.


Все стадии жизненного цикла H. nana проходят в организме человека. Человек — одновременно окончательный и промежуточный хозяин. Инфицирование наступает при проглатывании яиц через загрязненные фекалиями руки, овощи, фрукты или зелень.
Этапы жизненного цикла:


Этапы жизненного цикла:
Инфекции, вызванные H. nana и H. diminuta, чаще протекают бессимптомно. Тяжелые инфекции, вызванные H. nana, могут привести к болям в животе и диарее.
Диагноз ставится на основании обнаружения яиц в образцах кала. Методы концентрирования и повторные исследования повышают чувствительность микроскопии.
Дипилидиоз — паразитарное заболевание, вызываемое ленточным червем Dipylidium caninum (огуречный цепень).
D. caninum — двупористый ленточный червь из отряда Cyclophyllidea и семейства Dipylidiidae, который может паразитировать в кишечнике человека.
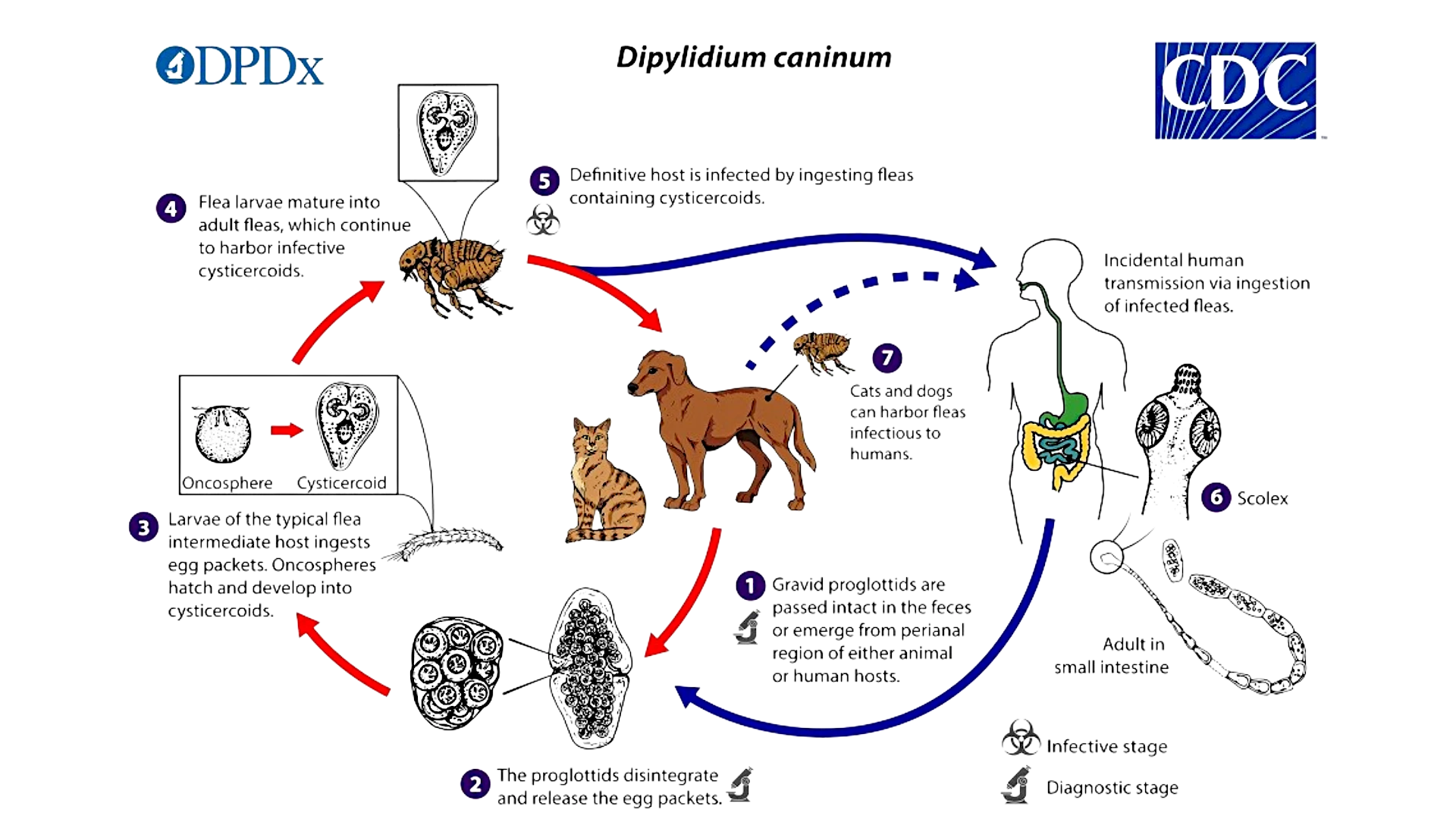

Типичные окончательные хозяева — домашние животные (собаки и кошки) и дикие хищники. Промежуточные хозяева — блохи. Люди выступают в роли случайных носителей, при этом дети наиболее уязвимы к инфицированию из-за низких гигиенических навыков. Ключевой фактор риска заражения — контакт с домашними и дикими животными.
В тонком кишечнике хозяина цистицеркоидная личинка фиксируется к стенке с помощью сколекса. Сколекс червя очень узкий. Членики по мере созревания увеличиваются в размерах.
Взрослый гельминт имеет беловатый цвет, длину 10–70 см и состоит из цепочки сегментов (проглоттид), независимых друг от друга.
В течение 2–3 недель (препатентный период) яйценосные членики, наполненные яйцами, отделяются и выводятся с фекалиями. Эти членики имеют форму и размеры семени огурца (отсюда название возбудителя — «огуречный цепень») или зерна риса. Сразу после выделения членики подвижны.
Яйца содержат первую личиночную стадию — гексакантовый эмбрион.
D. caninum встречается на всех континентах, кроме Антарктиды. Распространенность выше в сельской или пригородной местности. Паразит обнаруживается у позвоночных и насекомых.
Проглатывание инфицированной блохи приводит к развитию бессимптомного самокупирующегося заболевания (разрешается спонтанно в течение 6 недель), при этом в кале могут быть заметны проглоттиды взрослого гельминта. Редко заболевание может сопровождаться легкими неспецифическими симптомами, такими как боль и дискомфорт в животе, вздутие, диарея или запор, зуд в перианальной области.
Диагностика основывается на микроскопии кала с применением методов обогащения, а также на визуализации члеников в кале.
Профилактика включает лечение домашних собак от блох и избегание контакта с бездомными животными.
Предпочтительные режимы
В течение 3 дней после терапии кал должен быть исследован для поиска сколекса в качестве критерия излечения (невышедший сколекс регенерирует взрослого червя), а затем повторно через 1 и 3 месяца.
Альтернативные схемы
Первичные режимы
Альтернативные схемы
Дополнительные рекомендации
1. Что такое цестоды и кто из плоских червей относится к этому классу?
2. Что такое цестодозы?
3. Как протекает жизненный цикл цестод?
4. Какие симптомы вызывают цестоды у человека?
5. Какие препараты применяют для лечения цестодозов у человека?
Список источников
1.
VOKA 3D Anatomy & Pathology — Complete Anatomy and Pathology 3D Atlas [Internet]. VOKA 3D Anatomy & Pathology.
Available from: https://catalog.voka.io/
2.
CDC — DPDX — Taeniasis [Internet].
Available from: https://www.cdc.gov/dpdx/taeniasis/index.html
3.
Robertson Q, Ferraro M, Chen X, Buathong S, Rugilo C, Punpichet M, et al. Neuroparasitic infections: imaging features and diagnostic algorithms. British Journal of Radiology [Internet]. 2025 Jun 9;98(1172):1197–1208.
Available from: https://doi.org/10.1093/bjr/tqaf126
4.
Singh G, Chomba M, Sander JW. Neurocysticercosis: current diagnostic and treatment paradigms. Current Opinion in Neurology [Internet]. 2025 Jun 20;38(4):380–387.
Available from: https://doi.org/10.1097/wco.0000000000001396
5.
CDC — DPDX — Hymenolepiasis [Internet].
Available from: https://www.cdc.gov/dpdx/hymenolepiasis/index.html
6.
CDC — DPDX — Diphyllobothriasis [Internet].
Available from: https://www.cdc.gov/dpdx/diphyllobothriasis/index.html
7.
Durrani MI, Basit H, Blazar E. Diphyllobothriasis (Fish tapeworm infection) [Internet]. StatPearls — NCBI Bookshelf. 2023.
Available from: https://www.ncbi.nlm.nih.gov/books/NBK540971/
8.
Garcia HH, Gonzales I, Lescano AG, Bustos JA, Zimic M, Escalante D et al. Efficacy of combined antiparasitic therapy with praziquantel and albendazole for neurocysticercosis: a double-blind, randomised controlled trial. The Lancet Infectious Diseases [Internet]. 2014 Jul 3;14(8):687–695.
Available from: https://doi.org/10.1016/s1473-3099(14)70779-0
9.
Abraham A, Bustos JA, Carabin H, De Meijere R, Sahu PS, Rajshekhar V et al. The effectiveness of anti-inflammatory and anti-seizure medication for individuals with single enhancing lesion neurocysticercosis: A meta-analysis and expert group-based consensus recommendations. PLoS Neglected Tropical Diseases [Internet]. 2021 Mar 31;15(3):e0009193.
Available from: https://doi.org/10.1371/journal.pntd.0009193
10.
Coyle CM, Bustos JA, Del Brutto OH, Garcia HH, Nash TE, Rajshekhar V. Calcified neurocysticercosis: Understanding dead (Not necessarily inactive) parasites. American Journal of Tropical Medicine and Hygiene [Internet]. 2025 Mar 18;112(6):1187–1192.
Available from: https://doi.org/10.4269/ajtmh.24-0446
11.
Rousseau J, Castro A, Novo T, Maia C. Dipylidium caninum in the twenty-first century: epidemiological studies and reported cases in companion animals and humans. Parasites & Vectors [Internet]. 2022 May 9;15(1):131.
Available from: https://doi.org/10.1186/s13071-022-05243-5
12.
CDC — DPDx — Dipylidium caninum [Internet].
Available from: https://www.cdc.gov/dpdx/dipylidium/index.html
Резюме статьи с помощью ИИ
Выберите желаемого помощника ИИ:
Ссылка успешно скопирована
Спасибо!
Ваше сообщение отправлено!
Наши специалисты свяжутся с вами в ближайшее время. Если у вас возникли дополнительные вопросы, пожалуйста, свяжитесь с нами по адресу info@voka.io.