Базисный мониторинг во время анестезии: стандарты и обязательные параметры мониторинга
Разбор стандартов базисного мониторинга во время анестезии. Обязательные показатели оксигенации, вентиляции и гемодинамики для безопасности пациента.
Специальности
АкушерствоАнгиологияАнестезиологияГастроэнтерологияГематологияГепатологияГинекологияГистологияДерматологияИнфекционные болезниКардиологияНеврологияОнкологияОртопедияОториноларингологияОфтальмологияПедиатрияПульмонологияСтоматологияТравматологияУрологияФизиологияЭмбриологияЭндокринологияЭта статья предназначена только для информационных целей
Содержание этого сайта, включая текст, графику и другие материалы, предоставляется исключительно в информационных целях. Оно не является советом или руководством к действию. По поводу вашего конкретного состояния здоровья или лечения, пожалуйста, проконсультируйтесь с вашим лечащим врачом.
Спинальная, или субарахноидальная анестезия (СА) – это метод нейроаксиальной анестезии, при которой местный анестетик (с или без использования адъювантов) вводится в спинномозговую жидкость поясничного отдела позвоночника с целью получения предсказуемого сенсорного и моторного блока за счет воздействия на корешки спинномозговых нервов и спинальные структуры, отходящие от спинного мозга. Спинальная анестезия используется для анестезии и/или анальгезии при различных вмешательствах на позвоночнике, нижней части живота, тазу, промежности, а также нижних конечностях.
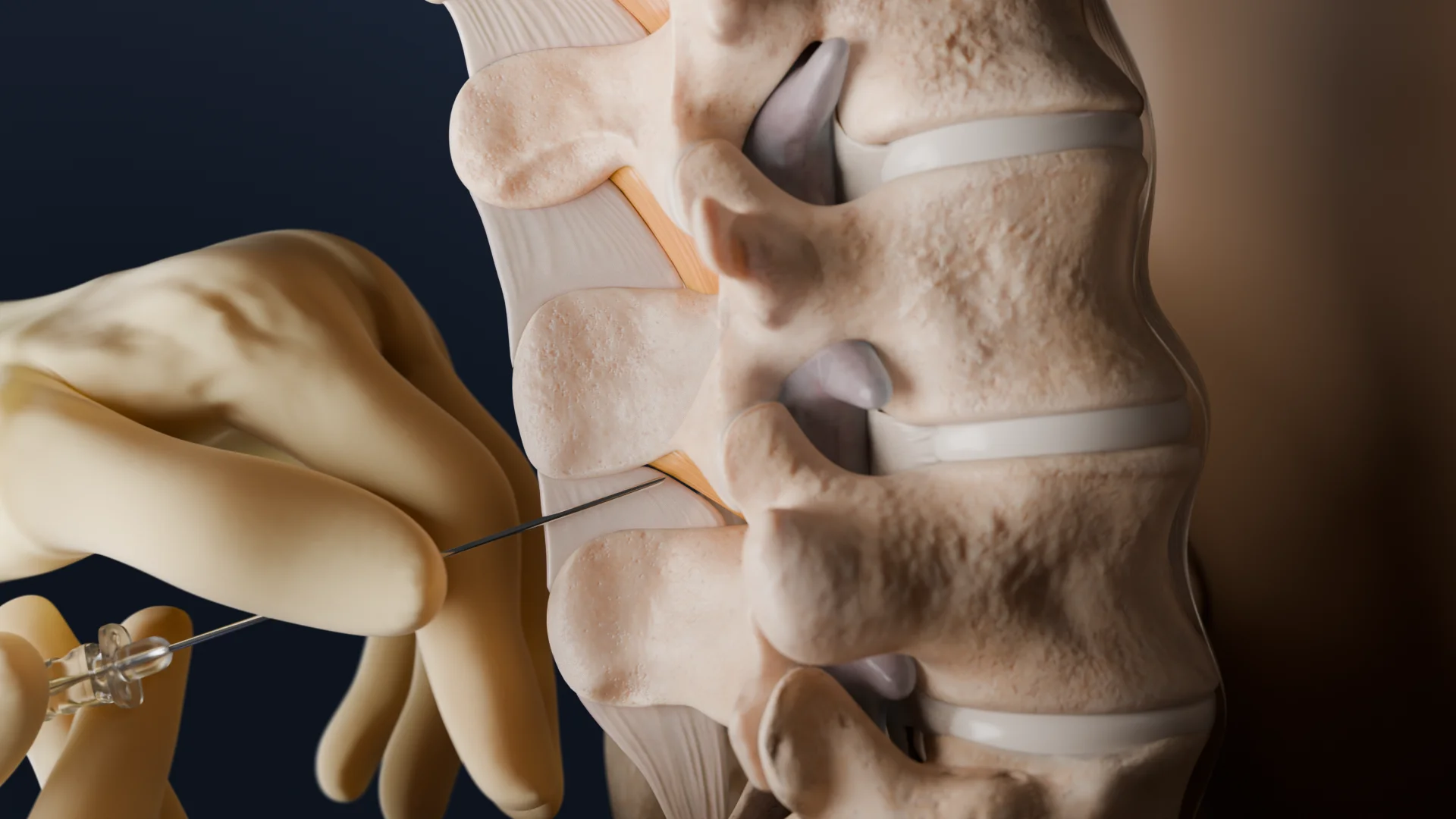

Спинальная анестезия может использоваться, как единственный метод, а также в сочетании с общей анестезией (ОА) для процедур на нижней половине тела:
Спинальная анестезия (СА) – это не только “техника пункции”, но прежде всего управляемое вмешательство в вегетативные и проводниковые механизмы организмы. Понимание функциональной анатомии позвоночника, оболочек спинного мозга и субарахноидального пространства, а также физиологических эффектов симпатической, сенсорной и моторной блокады позволяет прогнозировать распространение блока и предупреждать осложнения. Анатомо-физиологическая грамотность напрямую связана с безопасностью пациента и предсказуемостью результата.
Проведение спинальной анестезии требует от специалиста знания функциональной анатомии спинального блока, что невозможно без глубоких знаний о строении позвоночника, спинного мозга и спинномозговых нервов.




1. Кожа;
2. Подкожная жировая ткань;
3. Надостистая связка;
4. Межостистая связка;
5. Желтая связка;
6. Твердая мозговая оболочка;
7. Субдуральное пространство;
8. Паутинная оболочка;
9. Субарахноидальное пространство.
1. Кожа;
2. Подкожная жировая ткань;
3. Параостистые мышцы;
4. Желтая связка;
5. Твердая мозговая оболочка;
6. Субдуральное пространство;
7. Паутинная оболочка;
8. Субарахноидальное пространство.
СА вызывает блокаду симпатических, сенсорных и моторных волокон, компенсаторных рефлексов и ваготонию. С клинической точки зрения важно, что уровень симпатической блокады, как правило, превышает уровень сенсорной, следовательно, гемодинамические изменения могут возникать раньше и проявляться более выраженнее, чем ожидается по кожному уровню чувствительности.
Гипотензия и брадикардия являются наиболее распространенными и важными физиологическими эффектами нейроаксиальной анестезии, возникающие в результате симпатической блокады.
Блокада симпатических нервов вызывает гипотензию за счет воздействия на преднагрузку, постнагрузку, сократительную способность и частоту сердечных сокращений. Иными словами снижение системного сосудистого сопротивления и уменьшение венозного возврата приводят к гипотензии.
Дополнительные факторы риска возникновения гипотензии являются беременность, предшествующая гиповолемия и кровопотеря, возраст старше 40, ожирение, хроническое употребление алкоголя и артериальная гипертензия.
Частота сердечных сокращений вследствие СА может увеличиваться (как результат гипотензии) или уменьшаться (вследствие блокады симпатических волокон, либо из-за снижения венозного возврата — рефлекс Бейнбриджа, а также в результате возникновения рефлекса Безольда-Яриша — стимуляции механорецепторов левого желудочка).
Факторами риска брадикардии являются более молодой возраст, сердцебиение с частотой менее 60 в минуту, класс I по классификации ASA, терапия бета-адреноблокаторами, а также пролонгированный интервал PR на ЭКГ.
У пациентов с нормальной функцией легких спинальная анестезия оказывает незначительное влияние на функцию легких. Минутная вентиляция легких (МВЛ), объем мертвого пространства, фракция шунта и газовый состав артериальной крови меняются незначительно.
При высоком спинальном блоке может быть затруднен выдох из-за паралича межреберных и грудных мышц (снижается максимальная МВЛ и резервный объем выдоха). Следовательно, пациенты с обструктивными заболеваниями легких, для адекватной вентиляции которых используется вспомогательная мускулатура, должны находиться под более тщательным наблюдением после спинальной блокады. Пациенты с нормальной функцией легких и высоким спинальным блоком могут жаловаться на одышку (чаще всего обусловлена неспособностью ощущать движение грудной клетки во время акта дыхания — разъяснение ситуации помогает облегчить состояние пациента).
Поскольку высокая СА обычно не затрагивает шейный отдел позвоночника, сохраняется функция диафрагмального нерва и диафрагмы.
Показатели газового состава артериальной крови не изменяются во время высокой СА у пациентов, дышащих спонтанно воздухом комнатной температуры.
Вазодилатации и снижение системного сосудистого сопротивления приводят к повышению теплопотерь и ознобу, что требует активных методов согревания пациента (наружный обогрев и использование подогревателей жидкостей для внутривенного введения), как и во время общей анестезии.
Практическая последовательность процедуры предполагает следующие шаги:
Используются положения сидя и на боку с максимальным сгибанием поясницы, выбор которых зависит от предпочтений врача, планируемого положения пациента во время хирургической процедуры, телосложения пациента и его комфорта. Врач может выполнять процедуру сидя или стоя. В редких случаях используется прон-позиция в положении «складного ножа» (лежа на животе с согнутыми ногами) при некоторых проктологических или операциях на промежности. Для этих процедур предпочтительно использовать гипобарический или изобарический раствор местного анестетика.
Проводится обработка кожи антисептическим раствором (например 0.5% хлоргексидин). Раствор должен полностью высохнуть перед дальнейшим проведением процедуры.
В запланированное место пункции вводится небольшое количество местного анестетика (1% раствор лидокаина), инфильтрируют кожу и подкожную клетчатку.
В случае возникновения трудностей пальпации анатомических ориентиров рекомендовано предоперационное ультразвуковое исследование пациента.
Использование игл малого диаметра (24-27 G) и игл с закругленными, нережущими скосами снижает частоту возникновения постпункционной головной боли.
При срединном доступе игла-проводник вводится под небольшим краниальным углом до ощущения более плотной ткани, что указывает на то, что кончик иглы находится в межостистой связке.
Далее спинальная игла вводится в иглу-проводник. Игла проходит через желтую связку, затем через эпидуральное пространство, а затем через твердую мозговую оболочку. При прохождении иглы через каждый из этих слоев ощущается изменение сопротивления. Часто при проколе твердой мозговой оболочки ощущается «щелчок». Глубина проникновения иглы от кожи до твердой мозговой оболочки у пациентов с нормальным телосложением составляет 5,0±1,0 см.
После появления «щелчка» или потери сопротивления, следует извлечь стилет и, при правильном выполнении манипуляции, спинномозговая жидкость (СМЖ) начнет вытекать через наконечник иглы. Отток через иглы меньшего диаметра может быть очень медленным, особенно если пациент находится в положении на боку.
Если оттока нет, так как игла может быть закупорена нервным корешком, следует осуществить поворот иглы на 90°.
После обеспечения свободного оттока СМЖ следует медленно ввести местный анестетик со скоростью не более 0,5 мл/секунду. После завершения введения интродьюсер и спинальная игла извлекаются из спины пациента.
Спинальная анестезия обычно вводится в виде одной инъекции. Непрерывная спинальная анестезия через катетер, установленный в субарахноидальном пространстве, утратила актуальность из-за частоты неврологических осложнений (синдром конского хвоста), а также высокого риска постпункционной головной боли.
Включает в себя оценку сенсорного и моторного блоков, а также готовность справиться с потенциальными побочными эффектами, такими как гипотензия, брадикардия.
При необходимости следует использовать седативные препараты для достижения оптимального эффекта, чтобы снизить тревогу пациента, учитывая прямое седативное действие, возникающее в результате СА.
При СА необходимо выбирать местные анестетики и адъюванты таким образом, чтобы достичь требуемого уровня спинальной анестезии, а также обеспечить необходимую продолжительность анестезии на время хирургического вмешательства.
Наиболее важными факторами, определяющими степень сенсорной блокады, являются доза и баричность (это отношение плотности раствора к плотности СМЖ, соответственно анестетики делятся на гипер-, изо- и гипобарические) анестезирующего раствора.
Баричность влияет на распределение анестезирующего раствора в субарахноидальном пространстве: гипербарические растворы имеют тенденцию «опускаться» в СМЖ относительно места инъекции, а гипобарические растворы поднимаются выше места инъекции.
Гипербарические растворы приводят к более быстрому началу действия, большей степени сенсорной блокады и меньшей продолжительности действия по сравнению с изобарическими растворами. Следует учитывать, что местные анестетики нейротоксичны в высоких концентрациях.
Интратекальные опиоиды могут быть добавлены для улучшения интраоперационной и послеоперационной анальгезии:
α2-агонисты усиливает сенсорную и моторную блокады, продлевают продолжительность действия и способствуют послеоперационной анальгезии, воздействуя на альфа-адренергические рецепторы в спинном мозге:
К ожидаемым осложнениям относятся гипотензия и брадикардия в результате симпатической блокады, тошнота (поэтому следует профилактировать введением противорвотных препаратов), дискомфорт пациента в результате моторного и сенсорного блока, а также озноб.
1. Что такое спинальная анестезия?
2. Как долго продолжается действие спинальной анестезии?
3. Сколько времени требуется для полного восстановления после процедуры?
4. Чем спинальная анестезия отличается от эпидуральной?
5. Какие операции чаще всего выполняют под спинальной анестезией?
6. Какие существуют абсолютные противопоказания к проведению спинальной анестезии?
7. Какие препараты используют чаще всего?
8. Почему после спинальной анестезии бывает гипотензия?
9. Что такое «высокий» или «тотальный» спинальный блок?
10. Что такое постпункционная головная боль и как снизить риск её возникновения?
11. Что такое ТНС и чем оно отличается от серьёзных осложнений?
12. Какие симптомы после операции требуют немедленного внимания?
Список источников
1.
VOKA 3D Anatomy & Pathology — Complete Anatomy and Pathology 3D Atlas [Internet]. VOKA 3D Anatomy & Pathology.
Available from: https://catalog.voka.io/
2.
Ledesma I., Stieger A., Luedi M.M. (2024). Spinal anesthesia in ambulatory patients. Curr Opin Anaesthesiol. 37(6):661-665. doi: 10.1097/ACO.0000000000001412.
3.
DeLeon A.M., Wong C.A. Spinal anesthesia: Technique. In: Post TW, ed. UpToDate [Internet]. Waltham (MA): UpToDate; 2025 [updated 2025 Jun 26; cited 2026 Jan].
4.
Kietaibl S., Ferrandis R., Godier A. (2022). Regional anaesthesia in patients on antithrombotic drugs. European Journal of Anaesthesiology 39(2):p 100-132. DOI: 10.1097/EJA.0000000000001600.
Резюме статьи с помощью ИИ
Выберите желаемого помощника ИИ:
Ссылка успешно скопирована
Спасибо!
Ваше сообщение отправлено!
Наши специалисты свяжутся с вами в ближайшее время. Если у вас возникли дополнительные вопросы, пожалуйста, свяжитесь с нами по адресу info@voka.io.